Обязательная маркировка лекарственных препаратов (видеоинструкция)
23 апреля 2019

С 1 февраля 2017 года на территории Российской Федерации идет эксперимент по маркировке лекарственных препаратов в соответствии с постановлением Правительства Российской Федерации от 24 января 2017 г. № 62.
Для реализации эксперимента разработана информационная система мониторинга движения лекарственных препаратов (ИС МДЛП) для медицинского применения.
Оператором ИС МДЛП назначен Центр развития перспективных технологий (ЦРПТ).
Подробная информация по маркировке лекарственных препаратов размещена на сайте системы Честный ЗНАК (https://честныйзнак.рф/business/projects/medicines/).
С 1 июля 2019 года начинается регистрация аптек и медицинских организаций в системе Честный ЗНАК для работы с препаратами из перечня высокозатратных нозологий.
С 1 октября 2019 года маркировка станет обязательной для препаратов из перечня высокозатратных нозологий.
Согласно требованиям Федерального закона №425- ФЗ от 28 декабря 2017года обязательная маркировка вводится с 1 января 2020 г.
Письмо руководителям учреждений здравоохранения
Письмо руководителям учреждений здравоохранения и руководителям отделов здравоохранения Администраций районов Санкт-Петербурга
Инструкция по формированию заявок на оснащение оборудованием и заполнению заявлений о присоединении к Договорам безвозмездного пользования движимым имуществом
Нормативно-правовое обеспечение ФГИС МДЛП
Федеральные законы:
- Федеральный закон от 26 декабря 2008 г. N 294-ФЗ "О защите прав юридических лиц и индивидуальных предпринимателей при осуществлении государственного контроля (надзора) и муниципального контроля";
- Федеральный закон от 12 апреля 2010 г. N 61-ФЗ "Об обращении лекарственных средств";
- Федеральный закон от 6 апреля 2011 г. N 63-ФЗ "Об электронной подписи";
- Федеральный закон от 28.12.2017 года № 425-ФЗ «О внесении изменений в Федеральный закон «Об обращении лекарственных средств»;
-Федеральный закон от 15.04.2019 № 58-ФЗ «О внесении изменений в Кодекс Российской Федерации об административных правонарушениях» (начала действия документа 01.01.2020)
- Статья 6.34. Несвоевременное внесение данных в систему мониторинга движения лекарственных препаратов для медицинского применения либо внесение в нее недостоверных данных.– Для должностных лиц штраф составит 5-10 тыс. рублей, для юр.лиц – 50-100 тыс. рублей.
Постановления Правительства Российской Федерации:
- Постановление Правительства РФ от 22 декабря 2011 г. N 1081 "О лицензировании фармацевтической деятельности";
- Постановление Правительства РФ от 6 июля 2012 г. N 686 "Об утверждении Положения о лицензировании производства лекарственных средств";
- Постановление Правительства РФ от 28.08. 2018 № 1018 «О внесении изменений в постановление Правительства РФ от 24.01.2017 № 62»;
- Постановление Правительства РФ от 14.12.2018 № 1556 «Об утверждении положения о системе мониторинга движения лекарственных препаратов для медицинского применения»;
- Постановление Правительства РФ от 14.12.2018 № 1557 «Об особенностях внедрения системы мониторинга движения лекарственных препаратов для медицинского применения»;
- Постановление Правительства РФ от 14.12.2018 № 1558 «Об утверждении правил размещения общедоступной информации, содержащейся в системе мониторинга движения лекарственных препаратов для медицинского применения, в информационно-телекоммуникационной сети “интернет”
(в том числе в форме открытых данных)»;
- Постановление Правительства РФ от 07.08.2019 № 1027 «О внесении изменения в постановление Правительства РФ от 24.01.2017 №62;
- Постановление Правительства РФ от 30.08.2019 № 1118 «О внесении изменений в Положение о системе мониторинга движения лекарственных препаратов для медицинского применения» (утвержденное постановлением Правительства РФ от 14.12.2018 № 1556);
- Распоряжение Правительства РФ от 28.04.2018 № 791-р «Об утверждении модели функционирования системы маркировки товаров средствами идентификации в Российской Федерации»;
- Распоряжение Правительства РФ от 14.12.2018 № 2828-р «Об определении ООО «Оператор-ЦРПТ» уполномоченным на осуществление функций оператора системы мониторинга движения лекарственных препаратов для медицинского применения».
Подробно ознакомиться с материалами документации можно на сайте оператора системы маркировки
Порядок регистрации в ИС МДЛП
Порядок регистрации в информационной системе мониторинга движения лекарственных препаратов (ИС МДЛП)
Для успешной подготовки к регистрации организациям в ИС МДЛП необходимо убедиться в выполнении следующих условий:
- Наличие усиленной квалифицированной электронной подписи (УКЭП), оформленной на руководителя организации (для резидентов Российской Федерации и представительств иностранных организаций на территории Российской Федерации).
Регистрация организации с УКЭП, оформленной на сотрудника, отличного от руководителя, не предусмотрена. Если у вашей организации нет УКЭП, то ее можно оформить в одном из удостоверяющих центров, аккредитованных Министерством цифрового развития, связи и массовых коммуникаций Российской Федерации. Перечень аккредитованных удостоверяющих центров можно найти по адресу: https://minsvyaz.ru/ru/activity/govservices/2
- 2. Полное соответствие ФИО руководителя и ИНН организации, указанные в УКЭП, сведениям, внесенным в ЕГРЮЛ/ЕГРИП/РАФП (для резидентов Российской Федерации и представительств иностранных организаций на территории Российской Федерации).
Проверить сведения в ЕГРЮЛ/ЕГРИП и РАФП можно на сайте ФНС России;
- если по результатам проверки выявлены несоответствия, требующие корректировок ЕГРЮЛ/ЕГРИП, порядок и условия внесения изменений можно найти на сайте ФНС России;
- если выявлены несоответствия в УКЭП, требуется ее переоформление.
- Наличие лицензии на медицинскую деятельность и/или фармацевтическую деятельность, зарегистрированной в соответствующем федеральном органе исполнительной власти (для российских производителей лекарственных средств и организаций, осуществляющих оборот лекарственных препаратов на территории Российской Федерации).
Проверить сведения о лицензиях можно:
- в Едином реестре лицензий в том числе лицензий, выданных органами государственной власти субъектов Российской Федерации в соответствии с переданным полномочием по лицензированию отдельных видов деятельности на сайте Росздравнадзора;
- при отсутствии лицензии в реестре необходимо обратиться в соответствующий федеральный орган исполнительной власти.
Важная информация
- Для юридического лица, являющегося резидентом Российской Федерации или представительством иностранной организации при первом входе в «Личный кабинет» необходимо использовать усиленную квалифицированную электронную подпись руководителя организации;
- В дальнейшем к работе с системой мониторинга движения лекарственных препаратов для медицинского применения можно подключать сотрудников организации.
Для регистрации в Личном кабинете участника ИС МДЛП, рекомендуется осуществить следующие действия:
Пройти на портал национальной системы цифровой маркировки.
Для этого в адресную строку веб-браузера необходимо ввести http://честныйзнак.рф/ (см. рисунок 1).
Рисунок 1- адресная строка веб-браузера Internet Explorer 11
После перехода по данной ссылке, откроется портал национальной системы цифровой маркировки (см. рисунок 2).
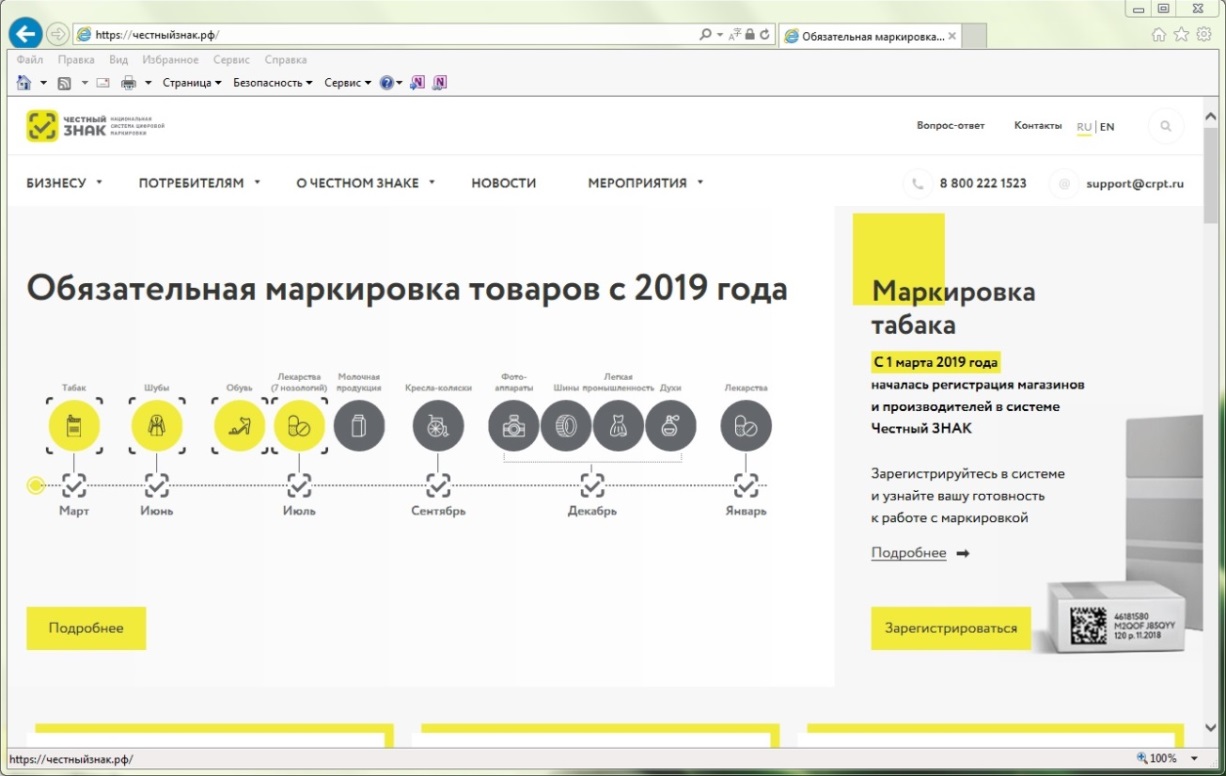
Рисунок 2 – Главная страница портала национальной системы цифровой маркировки
Далее надо перейти в раздел «Маркировка лекарств», с главной страницы портала цифровой маркировки это можно сделать, нажав на пиктограмму лекарств на временной шкале обязательной маркировки товаров (см. рисунок 3).
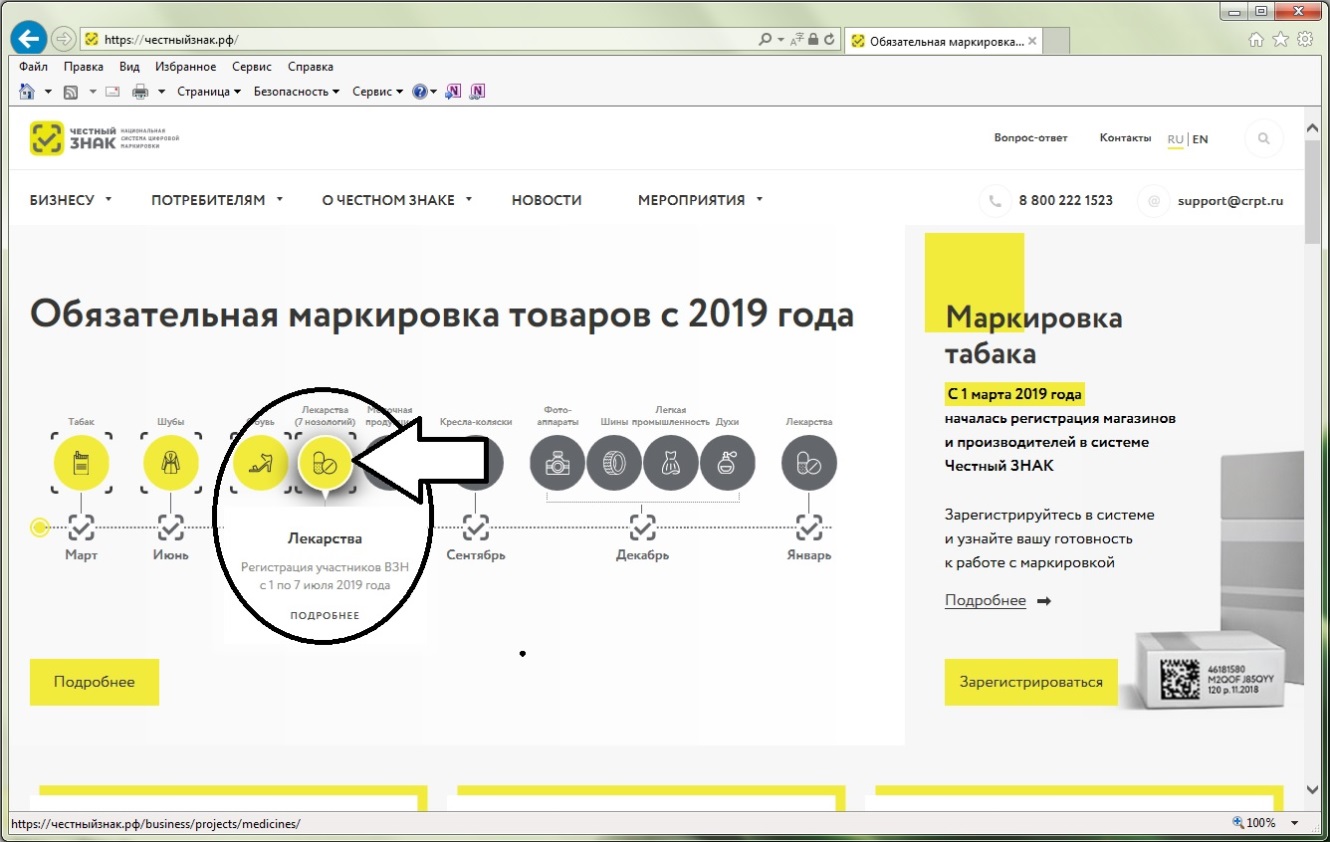
Рисунок 3 – Стрелкой выделена пиктограмма лекарственных препаратов, при нажатии на которую откроется раздел «Маркировка лекарств»
Вы перейдете в раздел «Маркировка лекарств». На данной странице представлена информация от национальной системы цифровой маркировки «Честный знак» в части маркировки лекарственных препаратов (см. рисунок 4).

Рисунок 4 – Раздел «Маркировка лекарств»
Для перехода на страницу регистрации в информационной системе мониторинга движения лекарственных препаратов (далее – ИС МДЛП) необходимо нажать под пиктограммой лекарственных препаратов на ссылку «Вход в систему».

Рисунок 5 – Стрелкой выделена ссылка на страницу входа в ИС МДЛП
Если ваше интернет-соединение медленное, скорее всего вы увидите следующее изображение (см. рисунок 6)
Рисунок 6 – скриншот анимации загрузки страницы входа в ИС МДЛП (отображается при медленном подключении к интернету)
На странице входа в систему необходимо нажать на ссылку для регистрации в системе (см. рисунок 7).
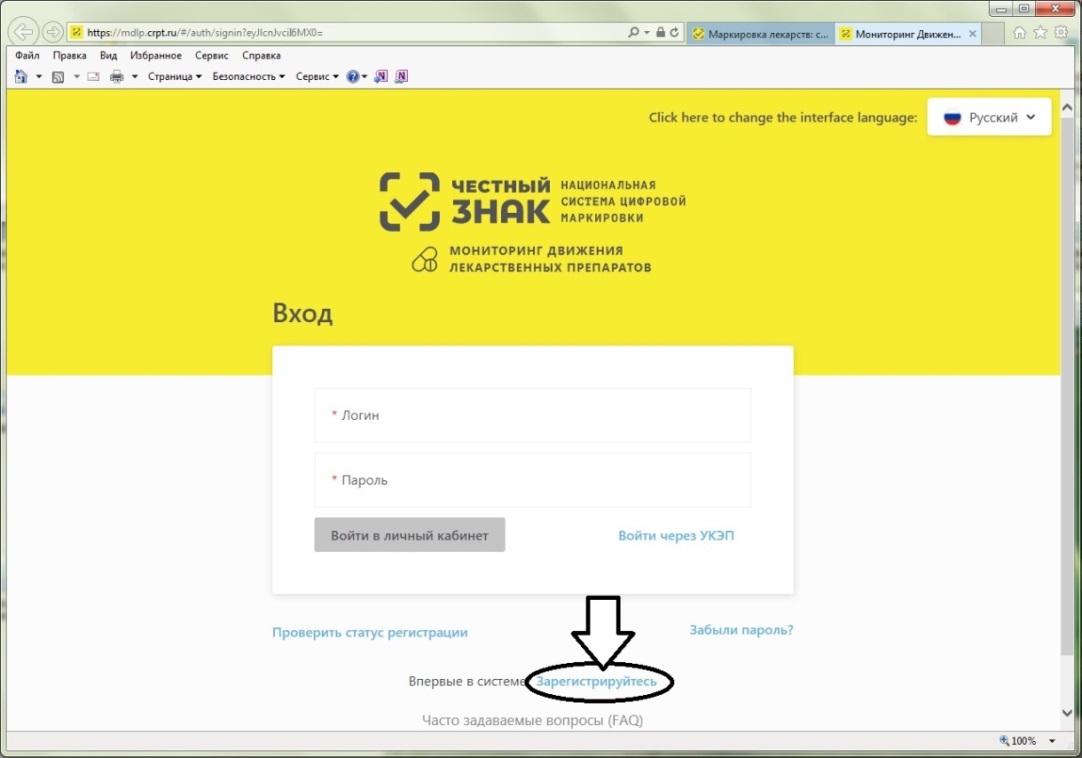
Рисунок 7 – Стрелкой выделена ссылка на регистрации в ИС МДЛП
Откроется окно регистрации в системе (см. рисунок 8).
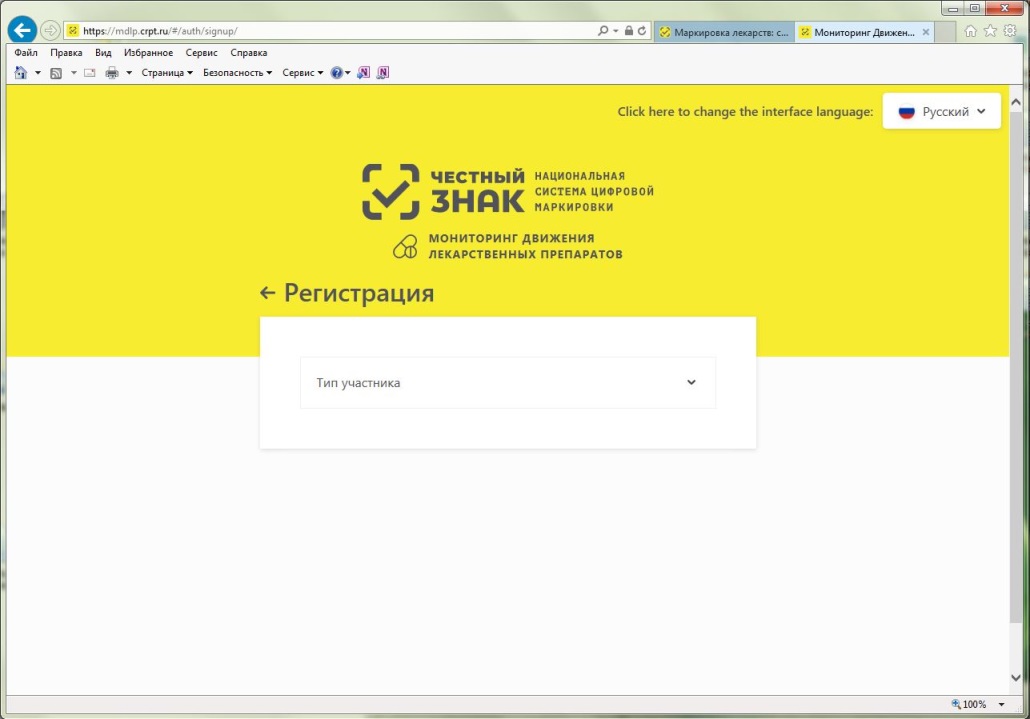
Рисунок 8 – Окно регистрации в ИС МДЛП
После выбора типа участника, система запросит необходимое программное обеспечение (см. рисунок 9).
Далее, при необходимости, следует установить программное обеспечение, сертификаты ключей электронной подписи и выполнить настройки программного обеспечения.

Рисунок 9 – ИС МДЛП запрашивает необходимое программное обеспечение для работы в системе.
Ниже представлены требования программного обеспечения в виде списка:
- операционная система Windows 7 (или более поздние),
либо MasOS X 10 (или более поздние); - браузеры:
- Internet Explorer 11 или более поздние (про режим предприятия и порядок его отключения см. приложение В);
- Safari 11.1 (13605.1.33.1.2) или более поздние;
- Chrome 66.0.3359.81 или более поздние;
- Mozilla Firefox 59.0.2 или более поздние;
- Opera 52 или более поздние
- Плагин средства криптографической защиты информации (СКЗИ) для браузера Internet Explorer / Safari. Список сертифицированных ФСБ СКЗИ доступен на сайте ФСБ
по адресу http://clsz.fsb.ru/certification.htm ; - Программное обеспечение выбранного Вами СКЗИ;
- Драйверы для работы с ключевыми носителями электронного ключа. Скачать драйвер и инструкцию по установке можно на сайте производителя СКЗИ.
Далее вам понадобится Руководство пользователя, откройте пункт 2 раздела 2.2.1 и следуйте дальнейшим инструкциям.
Материалы по МДЛП по Всероссийскому совещанию в Москве 11.09.2019 г. доступны по ссылке: http://www.roszdravnadzor.ru/pages/about/conference/markirovka

