Маркировка лекарственных препаратов (ИС – МДЛП)
Упрощённый порядок работы в системе маркировки и прослеживания лекарств в России продлевается ещё на 7 месяцев. Постановление об этом подписал Председатель Правительства Михаил Мишустин.
ИС "МДЛП" - Информационная система мониторинга движения лекарственных препаратов.
8-800-222-1435 Выделенная линия для аптек и медицинских организаций (Честный знак)
Нормативно-правовое обеспечение ФГИС МДЛП
Методические рекомендации:
Федеральные законы:
Федеральный закон от 12 апреля 2010 г. № 61-ФЗ "Об обращении лекарственных средств";
Федеральный закон от 6 апреля 2011 г. N 63-ФЗ "Об электронной подписи";
Федеральный закон от 15.04.2019 № 58-ФЗ «О внесении изменений в Кодекс Российской Федерации об административных правонарушениях» (начало действия документа 01.07.2020)
Постановления Правительства Российской Федерации:
Постановление Правительства РФ от 30.06.2020 N 955 «Об особенностях ввода в гражданский оборот лекарственных препаратов для медицинского применения» (срок действия документа ограничен 1 января 2021 года);
Постановление Правительства РФ от 26 ноября 2018 г. № 1416 «О порядке организации обеспечения лекарственными препаратами лиц, больных гемофилией, муковисцидозом, гипофизарным нанизмом, болезнью Гоше, злокачественными новообразованиями лимфоидной, кроветворной и родственных им тканей, рассеянным склерозом, гемолитико-уремическим синдромом, юношеским артритом с системным началом, мукополисахаридозом I, II и VI типов, лиц после трансплантации органов и (или) тканей, а также о признании утратившими силу некоторых актов Правительства Российской Федерации»;
Постановление Правительства РФ от 31.12. 2019 № 1954 «О внесении изменений в постановление Правительства РФ от 14.12.2018 № 1556»;
Постановление Правительства РФ от 14.12.2018 № 1558 «Об утверждении правил размещения общедоступной информации, содержащейся в системе мониторинга движения лекарственных препаратов для медицинского применения, в информационно-телекоммуникационной сети “Интернет” (в том числе в форме открытых данных);
Постановление Правительства РФ от 07.08.2019 № 1027 «О внесении изменения в постановление Правительства РФ от 24.01.2017 № 62;
Подробно ознакомиться с материалами документации можно на сайте оператора системы маркировки.
Порядок регистрации в ИС МДЛП
Порядок регистрации в информационной системе мониторинга движения лекарственных препаратов (ИС МДЛП)
Регистрация в информационной системе мониторинга движения лекарственных препаратов (ИС МДЛП)
Для успешной подготовки к регистрации организациям в ИС МДЛП необходимо убедиться в выполнении следующих условий:
- Наличие усиленной квалифицированной электронной подписи (УКЭП), оформленной на руководителя организации (для резидентов Российской Федерации и представительств иностранных организаций на территории Российской Федерации).
Регистрация организации с УКЭП, оформленной на сотрудника, отличного от руководителя, не предусмотрена. Если у вашей организации нет УКЭП, то ее можно оформить в одном из удостоверяющих центров, аккредитованных Министерством цифрового развития, связи и массовых коммуникаций Российской Федерации. Перечень аккредитованных удостоверяющих центров можно найти по адресу: https://minsvyaz.ru/ru/activity/govservices/2
- 2. Полное соответствие ФИО руководителя и ИНН организации, указанные в УКЭП, сведениям, внесенным в ЕГРЮЛ/ЕГРИП/РАФП (для резидентов Российской Федерации и представительств иностранных организаций на территории Российской Федерации).
Проверить сведения в ЕГРЮЛ/ЕГРИП и РАФП можно на сайте ФНС России.
- если по результатам проверки выявлены несоответствия, требующие корректировок ЕГРЮЛ/ЕГРИП, порядок и условия внесения изменений можно найти на сайте ФНС России;
- если выявлены несоответствия в УКЭП, требуется ее переоформление.
- Наличие лицензии на медицинскую деятельность и/или фармацевтическую деятельность, зарегистрированной в соответствующем федеральном органе исполнительной власти (для российских производителей лекарственных средств и организаций, осуществляющих оборот лекарственных препаратов на территории Российской Федерации).
Проверить сведения о лицензиях можно:
- в Едином реестре лицензий в том числе лицензий, выданных органами государственной власти субъектов Российской Федерации в соответствии с переданным полномочием по лицензированию отдельных видов деятельности на сайте Росздравнадзора;
- при отсутствии лицензии в реестре необходимо обратиться в соответствующий федеральный орган исполнительной власти.
Важная информация
- Для юридического лица, являющегося резидентом Российской Федерации или представительством иностранной организации при первом входе в «Личный кабинет» необходимо использовать усиленную квалифицированную электронную подпись руководителя организации;
- В дальнейшем к работе с системой мониторинга движения лекарственных препаратов для медицинского применения можно подключать сотрудников организации.
Для регистрации в Личном кабинете участника ИС МДЛП, рекомендуется осуществить следующие действия:
- Пройти на портал национальной системы цифровой маркировки. Для этого в адресную строку веб-браузера необходимо ввести https://честныйзнак.рф/ (см. рисунок 1).
Рисунок 1- адресная строка веб-браузера Internet Explorer 11
После перехода по данной ссылке, откроется портал национальной системы цифровой маркировки (см. рисунок 2).
Рисунок 2 – Главная страница портала национальной системы цифровой маркировки
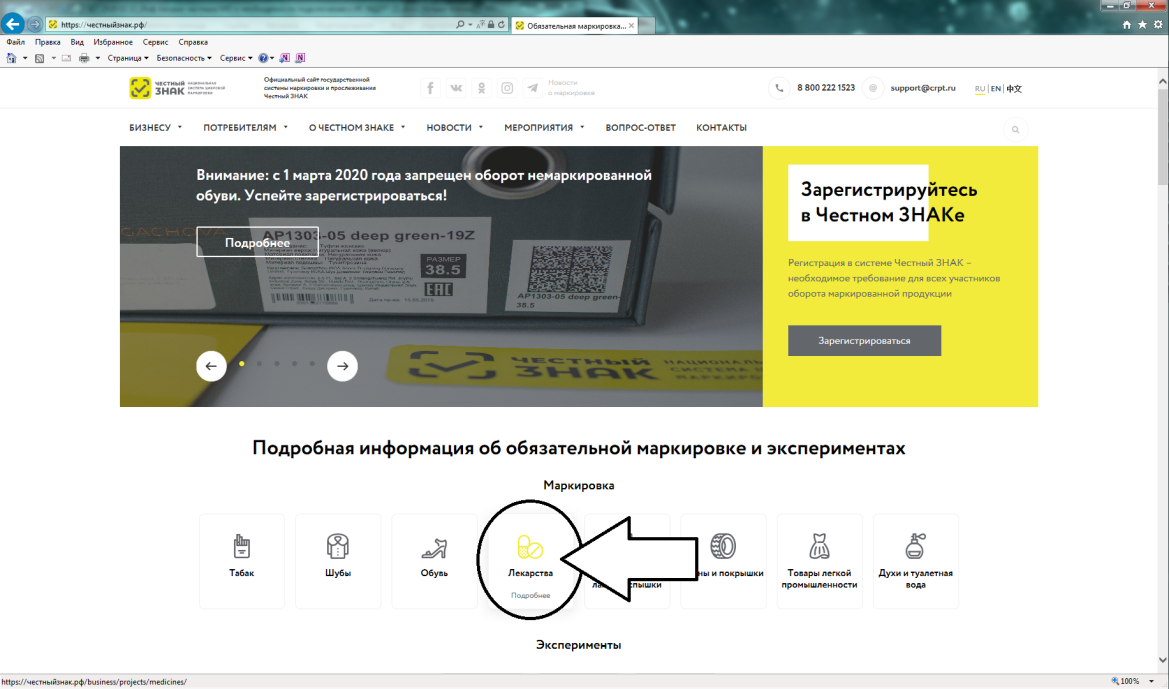
Далее надо перейти в раздел «Маркировка лекарств», с главной страницы портала цифровой маркировки это можно сделать, нажав на пиктограмму лекарств в блоке информации «Подробная информация об обязательной маркировке и экспериментах» – «Маркировка»(см. рисунок 3).
Рисунок 3 – Стрелкой выделена пиктограмма лекарственных препаратов, при нажатии на которую откроется раздел «Маркировка лекарств»
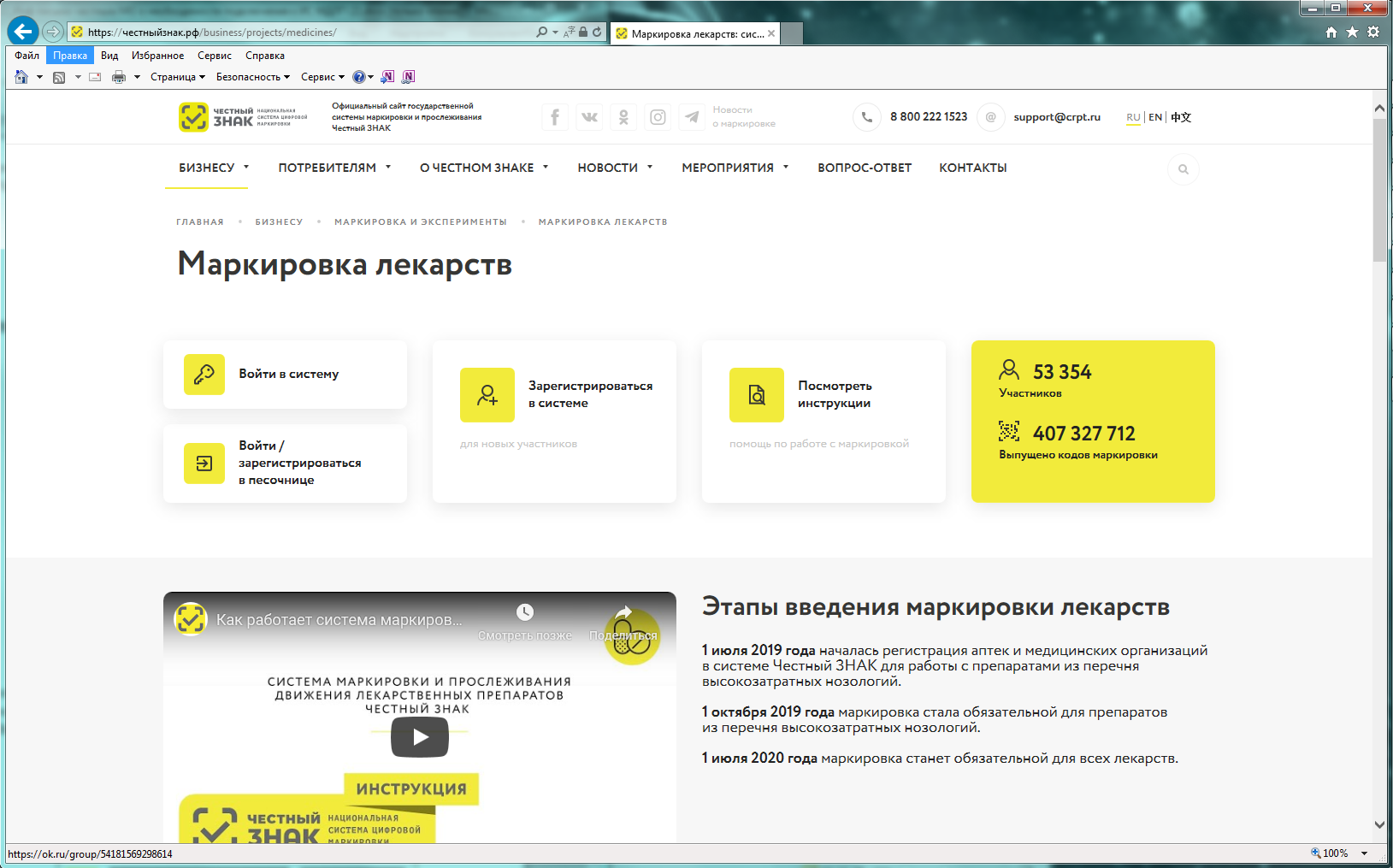
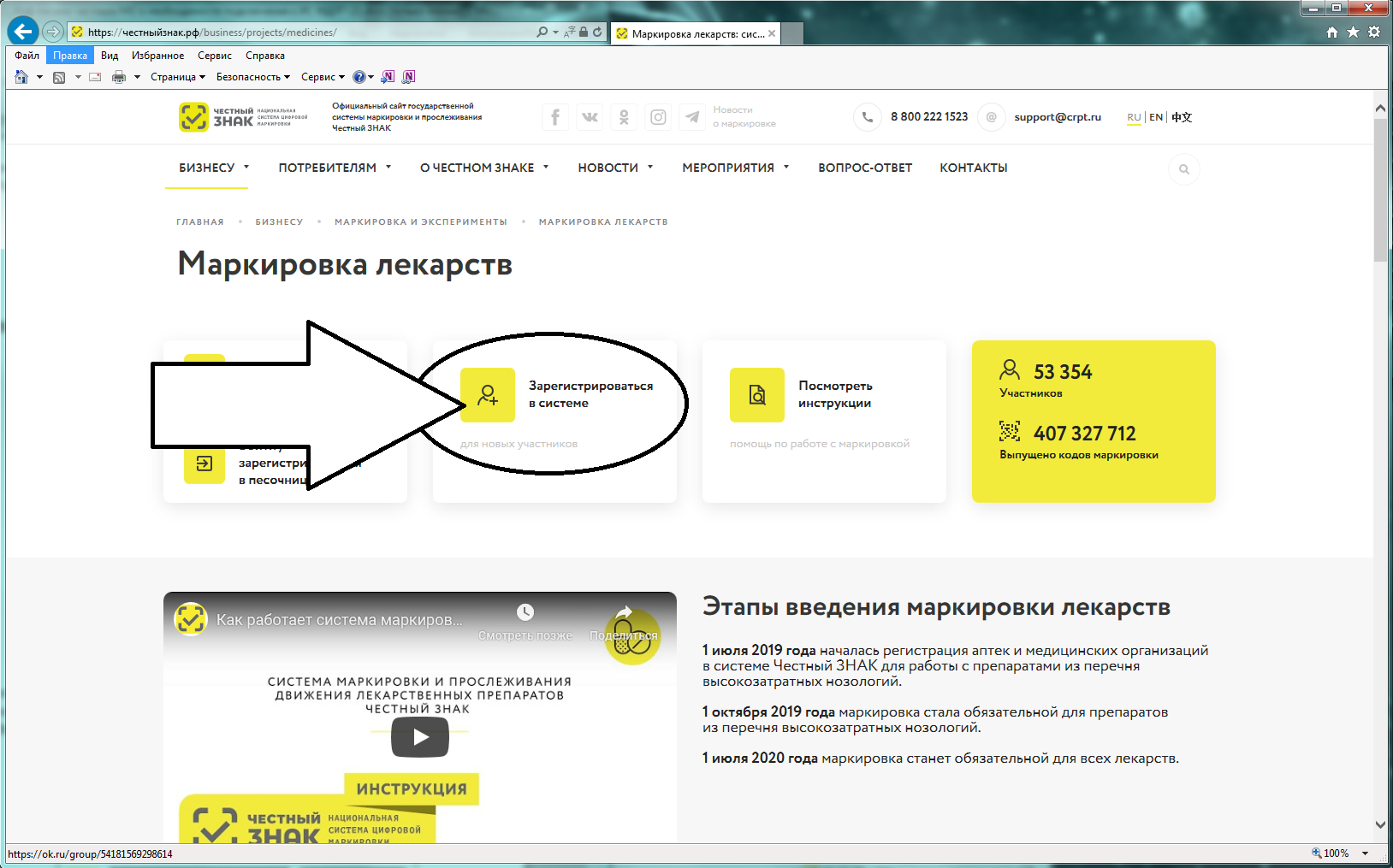
Вы перейдете в раздел «Маркировка лекарств». На данной странице представлена информация от национальной системы цифровой маркировки «Честный знак» в части маркировки лекарственных препаратов (см. рисунок 4).
Рисунок 4 – Раздел «Маркировка лекарств»
Для регистрации в информационной системе мониторинга движения лекарственных препаратов (далее – ИС МДЛП) необходимо нажать на кнопку с пиктограммой пользователя с плюсом и надписью «Зарегистрироваться в системе».
Рисунок 5 – Стрелкой выделена кнопка входа в ИС МДЛП
Если ваше интернет-соединение медленное, скорее всего вы увидите следующее изображение (см. рисунок 6)
 Рисунок 6 – скриншот анимации загрузки страницы входа в ИС МДЛП (отображается при медленном подключении к интернету)
Рисунок 6 – скриншот анимации загрузки страницы входа в ИС МДЛП (отображается при медленном подключении к интернету)
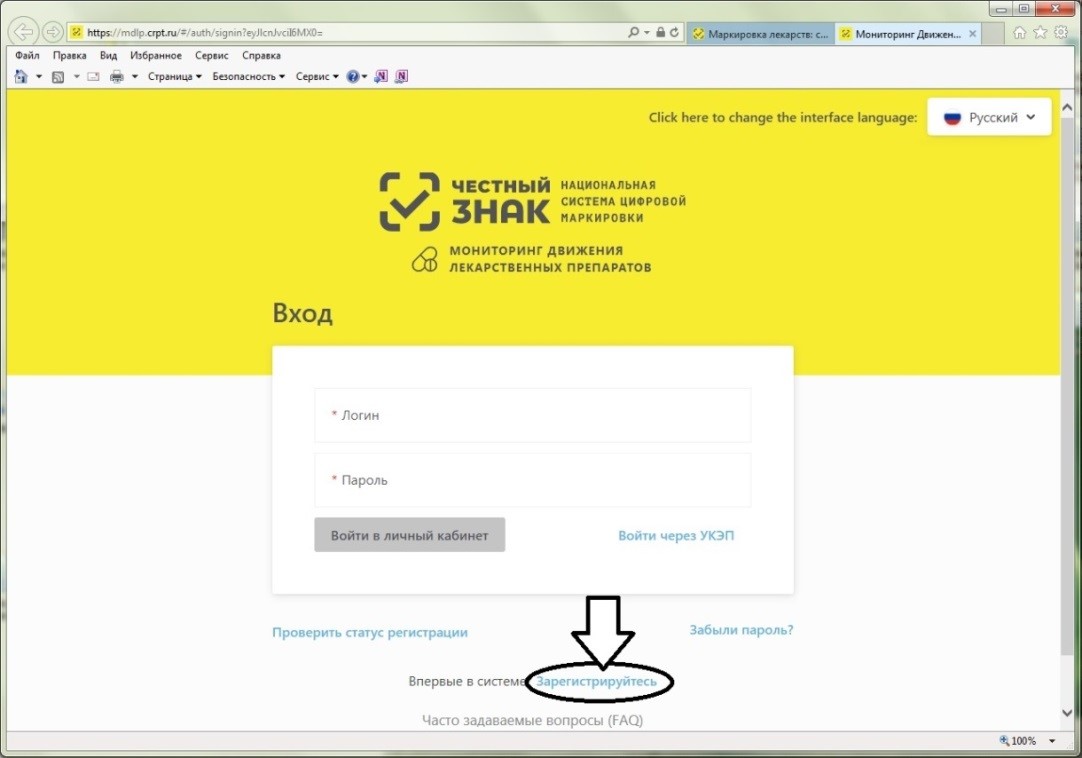
На странице входа в систему необходимо нажать на ссылку для регистрации в системе (см. рисунок 7).
Рисунок 7 – Стрелкой выделена ссылка для регистрации в ИС МДЛП
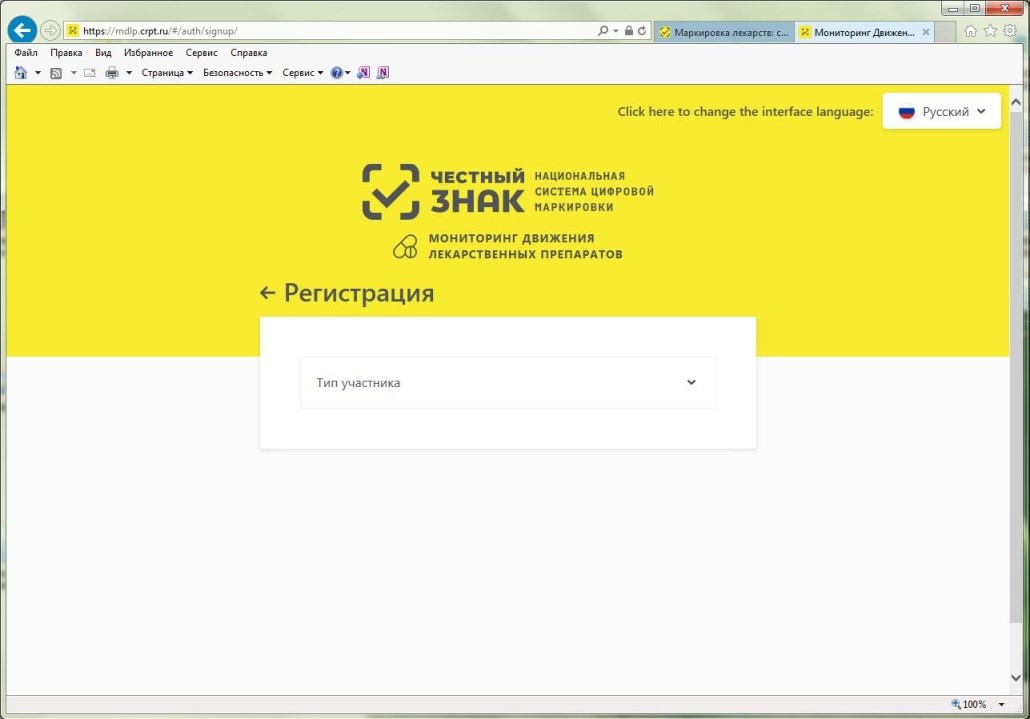
Откроется страница регистрации в системе (см. рисунок 8).
Рисунок 8 – Страница регистрации в ИС МДЛП
После выбора типа участника, система запросит необходимое программное обеспечение (см. рисунок 9).
Далее, при необходимости, следует установить программное обеспечение, сертификаты ключей электронной подписи и выполнить настройки программного обеспечения.
Рисунок 9 – ИС МДЛП запрашивает необходимое программное обеспечение для работы в системе.
Ниже представлены требования программного обеспечения в виде списка:
- операционная система Windows 7 (или более поздние),
либо MasOS X 10 (или более поздние); - браузеры:
- Internet Explorer 11 или более поздние (про режим предприятия и порядок его отключения см. приложение В);
- Safari 11.1 (13605.1.33.1.2) или более поздние;
- Chrome 66.0.3359.81 или более поздние;
- Mozilla Firefox 59.0.2 или более поздние;
- Opera 52 или более поздние
- Плагин средства криптографической защиты информации (СКЗИ) для браузера Internet Explorer / Safari. Список сертифицированных ФСБ СКЗИ доступен на сайте ФСБ
по адресу http://clsz.fsb.ru/certification.htm ; - Программное обеспечение выбранного Вами СКЗИ;
- Драйверы для работы с ключевыми носителями электронного ключа. Скачать драйвер и инструкцию по установке можно на сайте производителя СКЗИ.
Далее вам понадобится Руководство пользователя, откройте пункт 2 раздела 2.2.1 и следуйте дальнейшим инструкциям.
Обязательная регистрация в системе мониторинга движения лекарств для медицинского применения
Где получить информацию и задать вопросы о регистрации в cистеме мониторинга движения лекарственных препаратов